Ксантин
Материал из Википедии — свободной энциклопедии
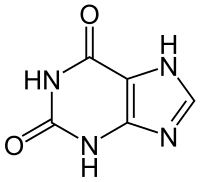
| Ксантин | |
|---|---|
 | |
| Общие | |
| Систематическое наименование |
3,7-Дигидропурин-2,6-дион |
| Хим. формула | C5H4N4O2 |
| Физические свойства | |
| Состояние | твёрдое (белый порошок) |
| Молярная масса | 152,11 г/моль |
| Термические свойства | |
| Температура | |
| • плавления | разлагается |
| Химические свойства | |
| Растворимость | |
| • в воде |
1 г/14,5 л при 16 °C 1 г/1,4 л при 100 °C |
| Классификация | |
| Рег. номер CAS | 69-89-6 |
| PubChem | 1188 |
| Рег. номер EINECS | 200-718-6 |
| SMILES | |
| InChI | |
| ChEBI | 17712 |
| ChemSpider | 1151 |
| Безопасность | |
| NFPA 704 | |
| Приведены данные для стандартных условий (25 °C, 100 кПа), если не указано иное. | |
Ксанти́н — пуриновое основание, обнаруживаемое во всех тканях организма. Бесцветные кристаллы, хорошо растворимые в растворах щелочей и кислот, формамиде, горячем глицерине и плохо растворимые в воде, этаноле и эфире.
История
[править | править код]Согласно статье В. А. Яковлева, опубликованной в «ЭСБЕ», ксантин был синтезирован Арманом Готье в 1884 году[1].
Свойства
[править | править код]Для ксантина характерна лактим-лактамная таутомерия и в водных растворах он существует в таутомерном равновесии с дигидроксиформой (2,6-дигидроксипурином) с преобладанием диоксоформы.
Имидазольный цикл ксантина нуклеофилен: ксантин галогенируется с образованием 8-галогенксантинов, азосочетание с солями диазония также идет с образованием 8-азоксантинов, которые затем могут быть восстановлены до 8-аминоксантина или гидролизованы до мочевой кислоты.
Ксантин проявляет амфотерные свойства, протонируясь по имидазольному азоту и образуя соли с минеральными кислотами (в том числе хорошо кристаллизующийся перхлорат), и образуя соли с металлами, катионы которых замещают кислые атомы водорода гидроксилов дигидроксиформы (например, нерастворимую серебряную соль реактивом Толленса).
В нейтральной среде ксантин метилируется диметилсульфатом по имидазольным атомам азота с образованием диметилпроизводного цвиттер-ионной структуры, в щелочной среде происходит депротонирование гидроксиформы с образованием высоконуклеофильных анионов, и, в зависимости от рН реакционной смеси, ксантин метилируется до 3,7-диметил-ксантина (теобромина), 1,3-диметилксантина (теофиллина) или 1,3,7-триметилксантина (кофеина).
Под действием оксихлорида фосфора происходит замещение гидроксильных групп дигидроксиформы ксантина на хлор с образованием 2,6-дихлорксантина, при действии пентасульфида фосфора в пиридине замещается только один из гидроксилов с образованием 6-тиоксантина.
Ксантин восстанавливается амальгамой натрия либо цинком в соляной кислоте до 6-дезоксиксантина, под действием перманганата калия в кислой среде ксантин окисляется с деградацией имидазольного цикла до 2,4,5,6-тетраоксопиримидина (аллоксана).
Метаболизм и нахождение в природе
[править | править код]Ксантин является продуктом катаболизма пуринов и образуется как продукт распада гуанина под действием гуаниндезаминазы и при окислении гипоксантина под действием ксантиноксидазы. Под действием той же ксантиноксидазы ксантин далее превращается в мочевую кислоту.
К производным ксантина относится целый ряд стимуляторов, таких как кофеин и теобромин. Абиогенный ксантин (наряду с урацилом) был обнаружен в метеорите Murchison.[2]
Патология
[править | править код]Редкое наследственное заболевание недостаточность ксантиноксидазы приводит к накоплению ксантина в организме и ксантинурии (появлению ксантина в моче).
См. также
[править | править код]Примечания
[править | править код]- ↑ Яковлев В. А. Готье, Арман // Энциклопедический словарь Брокгауза и Ефрона : в 86 т. (82 т. и 4 доп.). — СПб., 1890—1907.
- ↑ Martins, Zita; Oliver Botta, Marilyn L. Fogel Mark A. Sephton, Daniel P. Glavin, Jonathan S. Watson, Jason P. Dworkin, Alan W. Schwartz, Pascale Ehrenfreund. Extraterrestrial nucleobases in the Murchison meteorite (англ.) // Earth and Planetary Science Letters[англ.] : journal. Архивировано 10 августа 2011 года.
Основные типы алкалоидов | |
|---|---|
| Пирролидин | |
| Тропан | |
| Пиперидин | |
| Хинолизидин | |
| Пиридин | |
| Изохинолин | |
| Хинолин | |
| Индол | |
| Пурин | |
| Фенилэтиламин | |
| Терпены | |
| Другие | |
Text is available under the CC BY-SA 4.0 license; additional terms may apply.
Images, videos and audio are available under their respective licenses.

