Amonia kalcia nitrato
| Amonia kalcia nitrato | |||
 5 5
| |||
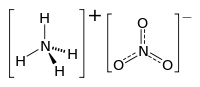
| Kemia strukturo de la Amonia kalcia nitrato | |||

| |||
| Kristaloj de amonia kalcia nitrato | |||

| |||
| Manko de nitrogeno en brasiko | |||
| GHS etikedigo de kemiaĵoj | |||
| GHS Damaĝo-piktogramo |
| ||
| GHS Signalvorto | Averto | ||
| GHS Deklaroj pri damaĝoj | H272, H319 | ||
| GHS Deklaroj pri antaŭgardoj | P210, P220, P221, P264, P280 | ||
Amonia kalcia nitrato, kalcia nitrato de amonio aŭ 5 Ca(NO3)2•NH4NO3•10H2O, ankaŭ konata kiel nitro-kalkoŝtono, estas grande uzata kiel neorganika sterko, respondante pri 4% el ĉiuj nitrogeno-sterkoj uzataj tutmonde. Kalcia amonia nitrato produktiĝas per aldono de kalcia karbonato al suspensaĵo da amonia nitrato.
La rezulta miksaĵo estas kalcia nitrato kaj rezidua amonia nitrato, kiu kristaliĝas kiel hidratigita duobla salo de amonio kaj kalcio. La konsumo de AKN ĉiujare estis 3,54 milionoj da tunoj en 1973/74, 4,45 milionoj da tunoj en 1983/84 kaj 3,58 milionoj da tunoj en 1993/94. Kalcia amonia nitrato estas higroskopa, ĝia dissolviĝo en akvo estas varmoeniga, rezultante ĝia uzo en kelkaj komercaj pakaĵoj por tuja malvarmigo.
Uzoj
[redakti | redakti fonton]Plejmulto el la amonia kalcia nitrato uzatas kiel kemia sterko. La AKN enhavas ĉirkaŭ 8% da kalcio kaj 21%-27% da nitrogeno. AKN prefereble uzatas en acidaj grundoj, pro tio ke ĝi acidigas la grundon malpli ol la ordinaraj nitrogeno-sterkoj. Ĝi same uzatas kiel anstataŭanto de la amonia nitrato, kie amonia nitrato estas malpermesata.
Aliflanke, AKN daŭre elmontras kreskantan uzon kiel improviza eksploda aparato. Laŭ raportoj, AKN kaj aliaj kemiaj sterkoj estas malpermesataj en Malakanda administracio, en Pakistano kaj Afganio, pro ĝia uzo kiel eksplodaĵo fare de la aktivistaj grupoj.
Reakcioj
[redakti | redakti fonton]Nitrato de kalcio kaj amonio verdire estas miksaĵo da substancoj kiuj povas prezenti la jenan konfiguracion:
aŭ depende de la kristaliĝaj kondiĉoj:
Industrie la miksaĵo estiĝas pere de miksaĵo de amonia nitrato kaj kalcia nitrato maldike pulvorigita. La miksaĵo devas efektiviĝi kiel eble plej rapide por eviti perdo de amoniako.
Literaturo
[redakti | redakti fonton]- Competition Science Vision Jan 2001
- The Fertilizer Encyclopedia, Vasant Gowariker, V. N. Krishnamurthy, Sudha Gowariker, Manik Dhanorkar, Kalyani Paranjape
- Producing Table Olives, Stan Kailis, David John Harris
- Australian Soil Fertility Manual
- Ammonium Nitrate: A Comparative Analysis of Factors Affecting Global Trade ...
- Fertigation with Microirrigation
- Growing Media for Ornamental Plants and Turf, Kevin A. Handreck, Neil D. Black
- Pollution Control in Fertilizer Production, C.A. Hodge
- Agricultural Nitrogen Use and Its Environmental Implications, Y. P. Abrol, Nandula Raghuram
| ||||||
Referencoj
[redakti | redakti fonton]Text is available under the CC BY-SA 4.0 license; additional terms may apply.
Images, videos and audio are available under their respective licenses.






