Natria telurito
| Natria telurito | ||
| ||
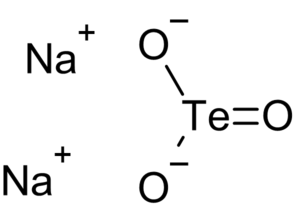
| Kemia strukturo de la Natria telurito | ||
| ||
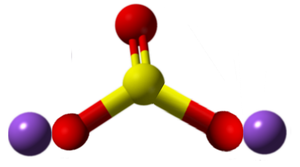
| 3D Kemia strukturo de la Natria telurito | ||

| ||
| Blankaj kristaloj de natria telurito | ||
| Kemia formulo | ||
| CAS-numero-kodo | 10102-20-2 | |
| ChemSpider kodo | 23309 | |
| PubChem-kodo | 24935 | |
| Fizikaj proprecoj | ||
| Aspekto | Blankaj kristaloj | |
| Molmaso | 221,57774 g mol−1 | |
| Smiles | [Na+].[Na+].[O-][Te]([O-])=O | |
| Denseco | 6,245 g/cm3 | |
| Fandopunkto | 710 °C (1,310 ℉; 983 K) | |
| Bolpunkto | malkonata (tre alta) | |
| Solvebleco | Akvo:100 g/ml | |
| Mortiga dozo (LD50) | 83 mg/kg (muso, buŝa) | |
| Merck Index |
| |
| Sekurecaj Indikoj | ||
| Risko | R23 R24 R25 | |
| Sekureco | S9 S20 S22 S36 S37 S39 S45 | |
| Pridanĝeraj indikoj | ||
| Danĝero
| ||
| GHS etikedigo de kemiaĵoj[1] | ||
| GHS Damaĝo-piktogramo |
| |
| GHS Signalvorto | Damaĝa substanco | |
| GHS Deklaroj pri damaĝoj | H300, H301, H311, H330, H331 | |
| GHS Deklaroj pri antaŭgardoj | P260, P261, P264, P270, P271, P280, P284, P301+310, P302+352, P304+340, P310, P311, P312, P320, P321, P330, P361, P403+233, P405, P501 | |
(25 °C kaj 100 kPa) | ||
Natria telurito, telurito de natrio aŭ Na2TeO3 estas neorganika oksokombinaĵo de natrio kaj teluro, blanka solido akvosolvebla kaj tre malforta reduktagento.[2] Ĝi estas peraĵo kaj antaŭaĵo en la ekstraktado de la elementa teluro per elektrolizo. Kiam hejtata ĝis malkomponiĝo, ĝi eligas toksajn telurajn fumojn kaj natrian oksidon.
Sintezoj
[redakti | redakti fonton]Sintezo 1
[redakti | redakti fonton]- Telurito de natrio prepariĝas sub alta temperaturo per interagado de arĝenta telurido kaj natria karbonato kune kun gasa oksigeno:
|
|
Sintezo 2
[redakti | redakti fonton]- Dissolvado de telura duoksido en diluita solvaĵo da natria hidroksido:
|
|
Sintezo 3
[redakti | redakti fonton]- Fando de telura duoksido kaj natria oksido:
|
|
Sintezo 4
[redakti | redakti fonton]- Dissolvado de teluroza acido en koncentrita solvaĵo da natria hidroksido:
|
|
Reakcioj
[redakti | redakti fonton]Reakcio 1
[redakti | redakti fonton]- Ĝi malkomponiĝas en akva medio laŭ neinversigebla maniero:
|
|
Reakcio 2
[redakti | redakti fonton]- Kun diluita acido ĝi estigas teluritan acidon:
|
|
Reakcio 3
[redakti | redakti fonton]- Per hejtado kaj diluita acido ĝi estigas teluran duoksidon:
|
|
Reakcio 4
[redakti | redakti fonton]- Sub la atmosfera oksigeno ĝi oksidiĝas al natria telurato:
|
|
Reakcio 5
[redakti | redakti fonton]- Interagado kun natria peroksido ĝi estigas natrian ortoteluraton:
|
|
Reakcio 6
[redakti | redakti fonton]- La sama reakcio kun natria peroksido en akvomedio rezultas en formado de dunatria kvarhidrogena telurato:
|
|
Reakcio 7
[redakti | redakti fonton]- Ĝi aktivas kiel oksidigagento:[3]
|
|
Reakcio 8
[redakti | redakti fonton]- Tamen, ĝi povas reakcii kiel reduktagento:
|
|
Strukturo
[redakti | redakti fonton]Teluro havas proprecojn similajn al sulfuro kaj seleno. En la anhidra formo, la teluratomoj en la molekulo havas 6 koordinatoj, tri Te-O kun 1,87 Å, kaj tri 2,9 Å kun distordaj okedraj dividantaj ekstremaĵoj, En la kvinhidrata modelo, Na2TeO3.5H2O, ekzistas diskretaj teluritaj anjonoj, TeO32−, kiuj estas piramidaj.
La interatomaj distancoj Te-O estas 1,85 Å kaj angulo O-Te-O proksima al 99,5°. La telurita anjono estas malforta bazo. Natria telurito strukture estas simila al natria selenito kaj natria sulfito. Telurito de natrio estas malforta oksidigagento kaj same malforta reduktagento.
Uzo
[redakti | redakti fonton]Telurito de natrio plibonas la reziston al korodaĵo sur metaldeponitaj nikel-tavoloj. Solvaĵoj de natria telurito uzatas por nigra kaj blua-nigraj elfinaĵoj sur fero, ŝtalo, aluminio kaj kupro. En mikrobiologio, natria telurito povas aldoniĝi en la kresko-medio por izolado de bakterio kun propra fiziologia rezisto al ĝia tokseco.
Literaturo
[redakti | redakti fonton]- Sigma Aldrich
- American Elements
- Toxnet
- Cameo Chemicals
- Chemical Book
- Tellurite Glasses Handbook: Physical Properties and Data, Raouf A.H. El-Mallawany
- The Relation of Selected Trace Elements to Health and Disease
| ||||||
Referencoj
[redakti | redakti fonton]- ↑ PubChem
- ↑ Tellurium in Organic Synthesis: Second, Updated and Enlarged Edition, Nicola Petragnani, Hélio A. Stefani
- ↑ Hazardous Metals in Human Toxicology, A. Vercruysse
Text is available under the CC BY-SA 4.0 license; additional terms may apply.
Images, videos and audio are available under their respective licenses.












![{\displaystyle {\mathsf {Na_{2}TeO_{3}+2\;Na[Sn(OH)_{3}]+3\;H_{2}O\ {\xrightarrow {NaOH))\ Te\downarrow +{\underset {natria\;ortotelurato}{2\;Na_{2}[Sn(OH)_{6}]))))}](https://wikimedia.org/api/rest_v1/media/math/render/svg/7e1893cb5e1dabd53d3cc3dd11b99242abbc70af)


