Natria telurato
| Natria metatelurato | |||
| |||
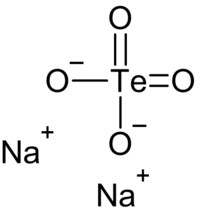
| Kemia strukturo de la Natria metatelurato | |||

| |||
| 3D Kemia strukturo de la Natria metatelurato | |||
| Kemia strukturo de Natria ortotelurato | |||
| 3D kemia strukturo de Natria ortotelurato | |||
| Alternativa(j) nomo(j) | |||
| |||
| Kemia formulo |
| ||
| CAS-numero-kodo | |||
| PubChem-kodo | 159260 | ||
| Aspekto | Senkoloraj kristaloj | ||
| Fizikaj proprecoj | |||
| Molmaso |
| ||
| Sekurecaj Indikoj | |||
| Risko | R23/24/25 R36/37/38 | ||
| Sekureco | S22 S26 S27 S36/37/39 S45 | ||
| Pridanĝeraj indikoj | |||
| Danĝero
| |||
| GHS etikedigo de kemiaĵoj | |||
| GHS Damaĝo-piktogramo |
| ||
| GHS Signalvorto | Damaĝa substanco | ||
| GHS Deklaroj pri damaĝoj | H261, H302, H312, H332, H315, H319 | ||
| GHS Deklaroj pri antaŭgardoj | P231+232, P305+351+338, P302+352, P321, P402+404, P501 | ||
(25 °C kaj 100 kPa) | |||
Natria telurato, telurato de natrio estas neorganika oksokombinaĵo de natrio kaj teluro, senkoloraj kristaloj, iomete solvebla en akvo, kiuj formas kristalajn hidratojn. La natriaj teluratoj prezentiĝas sub du formoj: natria metatelurato aŭ Na2Teo4, kaj natria orto-telurato aŭ Na6Teo6.
Ĝi prepariĝas same kiel la natria selenato kaj facile estas reduktita al teluro. Ĝia plej konata formo estas la duhidrata. Ĝi estas venena per ingestado, intraperitonea kaj intravejna vojoj. Kiam hejtata ĝis malkomponiĝo, ĝi liverigas toksajn telurajn fumojn kaj natrian oksidon[1].
Sintezoj
[redakti | redakti fonton]Sintezo 1
[redakti | redakti fonton]- Senhidratigo de dunatria kvarhidrogena telurato:
|
|
Sintezo 2
[redakti | redakti fonton]- Oksidigo de natria telurito:
|
|
Sintezo 3
[redakti | redakti fonton]- Natria telurato estiĝas pere de oksidigo de teluro, unue kun troo da nitrata acido, produktante teluratan acidon. La telurata acido estas neŭtraligata de natria karbonato:
|
|
Sintezo 4
[redakti | redakti fonton]- Dissolvado de teluro en koncentritaj alkalaj solvaĵoj kune kun hidrogena peroksido:
|
|
Sintezo 5
[redakti | redakti fonton]- Traktado de telurata acido kaj natria karbonato:
|
|
Sintezo 6
[redakti | redakti fonton]- Reakcio inter natria telurito kaj hidrogena peroksido:
|
|
Sintezo 7
[redakti | redakti fonton]- Oksidigo de natria telurito:
|
|
Sintezo 8
[redakti | redakti fonton]- Elektrolizo de solvaĵo da natria telurito:
|
|
Sintezo 9
[redakti | redakti fonton]- Neŭtraliga reakcio de telurata acido kaj natria hidroksido:
|
|
Sintezo 10
[redakti | redakti fonton]- Traktado de natria karbonato kun telurata acido:
|
|
Reakcioj
[redakti | redakti fonton]Reakcio 1
[redakti | redakti fonton]- Kiam hejtata, natria telurato malkomponiĝas:
|
|
Reakcio 2
[redakti | redakti fonton]- La kristala salo estiĝas per hejtado kaj vakua sekigo:
|
|
Reakcio 3
[redakti | redakti fonton]- Per traktado kun telurata acido ĝi estigas acidan salon de la respektiva acido:
|
|
Reakcio 4
[redakti | redakti fonton]- Ĝi estas forta oksidigagento:
|
|
Reakcio 5
[redakti | redakti fonton]- Per hidrogeno ĝi reduktiĝas al natria telurido:
|
|
Reakcio 6
[redakti | redakti fonton]- Ĝi partoprenas en reakcio pri duobla interŝanĝo kun baria klorido:
|
|
Reakcio 7
[redakti | redakti fonton]- Ĝi reakcias kun sulfura trioksido:[2]
|
|
Literaturo
[redakti | redakti fonton]
| ||||||
Referencoj
[redakti | redakti fonton]Text is available under the CC BY-SA 4.0 license; additional terms may apply.
Images, videos and audio are available under their respective licenses.




















