Izobutila sulfido
| Duizobutila sulfido | |||
 | |||
| Plata kemia strukturo de la Izobutila sulfido | |||
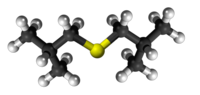 | |||
| Tridimensia kemia strukturo de la Izobutila sulfido | |||
| Alternativa(j) nomo(j) | |||
| |||
| Kemia formulo | |||
| CAS-numero-kodo | 592-65-4 | ||
| ChemSpider kodo | 11119 | ||
| PubChem-kodo | 11608 | ||
| Fizikaj proprecoj | |||
| Aspekto | senkolora, brulema, rapidbola kaj toksa likvaĵo kun penetranta odoro | ||
| Molmaso | 146,292 g·mol−1 | ||
| Denseco | 0,839g cm−3 | ||
| Fandpunkto | −105,5 °C[1] | ||
| Bolpunkto | 171 °C[2] | ||
| Refrakta indico | 1,445[1] | ||
| Ekflama temperaturo | 45,9 °C[3] | ||
| Solvebleco | Akvo:Malmulte solvebla | ||
| Mortiga dozo (LD50) | 2220 mg/kg (buŝe) | ||
| Sekurecaj Indikoj | |||
| Riskoj | R11 R38 | ||
| Sekureco | S9 S16 S26 S33 S36 | ||
| Pridanĝeraj indikoj | |||
| Danĝero
| |||
| GHS Damaĝo Piktogramo |
| ||
| GHS Signalvorto | Damaĝa substanco | ||
| GHS Deklaroj pri damaĝoj | H227, H301, H303, H305, H315, H319, H331, H335, H336 | ||
| GHS Deklaroj pri antaŭgardoj | P210, P233, P240, P241, P242, P243, P280, P303+361+353, P370+378, P403+235, P501[4] | ||
(25 °C kaj 100 kPa) | |||
Izobutila sulfido aŭ C8H18S estas kemia kombinaĵo, apartenanta al la funkcia grupo de la esteroj de la sulfida acido kaj izobutila alkoholo. Izobutila sulfido estas senkolora, brulema, rapidbola kaj toksa likvaĵo kun penetranta odoro, analiza reakciaĵo uzata en kemiaj sintezoj kaj en la fabrikado de kosmetikaĵoj kaj farmaciaĵoj. Kutime ĝi estiĝas per kondensiĝa reakcio aŭ per esterigo de Fischer-Speyer kun sulfata acido kiel katalizilo. Izobutila sulfido estas malmulte solvebla en akvo, sed tute solvebla en alkoholo, duetila etero, kloroformo kaj plejmulto el la organikaj solvantoj. Izobutila sulfido reakcias kun fortaj oksidigagentoj kaj fortaj bazoj. Sulfidaj esteroj malkomponiĝas per varmigo aŭ kun la tempopaso en sulfuro aŭ sulfuraj derivaĵoj.
Sintezoj
[redakti | redakti fonton]Sintezo 1
[redakti | redakti fonton]- Preparado per agado de sulfida acido kaj izobutila alkoholo:
Sintezo 2
[redakti | redakti fonton]- Preparado per traktado de natria sulfido kaj izobutila alkoholo:
Sintezo 3
[redakti | redakti fonton]- Preparado per reakcio de sulfida acido kaj izobutila klorido:
Sintezo 4
[redakti | redakti fonton]- Preparado per interagado de natria sulfido kaj izobutila klorido:[5]
Sintezo 5
[redakti | redakti fonton]- Preparado per interagado de metila sulfido kaj izobutila formiato:
Sintezo 6
[redakti | redakti fonton]- Preparado per acida transesterigo inter sulfida acido kaj izobutila benzoato:
Sintezo 7
[redakti | redakti fonton]- Preparado per traktado de duizobutil-sulfuroksido kaj jodida acido:
Reakcioj
[redakti | redakti fonton]Reakcio 1
[redakti | redakti fonton]- Hidrolizo de la izobutila sulfido:
Reakcio 2
[redakti | redakti fonton]- Sapigo de la izobutila sulfido:
Reakcio 3
[redakti | redakti fonton]- Reakcio per acida transesterigo kun formiata acido:
Reakcio 4
[redakti | redakti fonton]- Reakcio per alkohola transesterigo kun metila alkoholo:
Reakcio 5
[redakti | redakti fonton]- Reakcio per acida transesterigo kun benzoata acido:
Reakcio 6
[redakti | redakti fonton]- Reakcio kun NH3:
Reakcio 7
[redakti | redakti fonton]- Reakcio kun HCl:
Literaturo
[redakti | redakti fonton]- The Good Scents Company
- Cheméo
- Specific Intermolecular Interactions of Element-Organic Compounds
- International Critical Tables of Numerical Data, Physics, Chemistry ...
- 1998 Freshman Achievement Award
- CRC Handbook of Chemistry and Physics
- Chemistry of organic sulfur compounds in petroleum and petroleum products
- Patt's industrial hygiene and toxicology: Toxicology
Referencoj
[redakti | redakti fonton]
| ||||||
Text is available under the CC BY-SA 4.0 license; additional terms may apply.
Images, videos and audio are available under their respective licenses.




![{\displaystyle {\mathsf ((\xrightarrow[{\,}]{))\,))}](https://wikimedia.org/api/rest_v1/media/math/render/svg/3a133815724e6bf6cfb39eb43f1e6c1d96ea8d17)