多胺



多胺(英语:polyamines),又称多元胺,是一种具有两个或多个主要胺基(-NH2)的有机化合物。
这类的化合物包含一些合成物质,可以做为化学工业中重要的原料,像是乙二胺(H
2N–CH
2–CH
2–NH
2)、1,3-二氨基丙烷(H
2N–(CH
2)
3–NH
2)、六亚甲基二胺(H
2N–(CH
2)
6–NH
2)。它还包括许多物质可以在真核生物、原核生物中发挥重要的作用,例如腐胺(H
2N–(CH
2)
4–NH
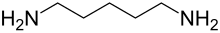
2)、尸胺(H
2N–(CH
2)
5–NH
2)、亚精胺(H
2N–(CH
2)
4–NH–(CH
2)
3–NH
2)、精胺(H
2N–(CH
2)
3–NH–(CH
2)
4–NH–(CH
2)
3–NH
2)。
截至2004年,没有发现任何的偕二胺在同一个碳原子上具有两个或多个–NH
2取代基团,但是取代的衍生物则是已知的,例如四乙基甲二胺((C
2H
5)
2N–CH
2–N(C
2H
5)
2)。[1]
功能
生物性
尽管已知多胺是在高度调节途径的细胞中被合成的,但他们的实际功能却还没完全解明。作为阳离子,他们和DNA结合,在结构上它们被发现与阳离子化合物在规则的间隔之间(不同于Mg2+
、Ca2+
,它们是点电荷)。它们也被发现可以作为转译过程中核糖体移码的启动子。[2]
如果细胞中多胺合成受到抑制,导致细胞生长停止或是严重延迟,则外源性多胺可以恢复这些细胞的生长。大多数的真核细胞的细胞膜上会有一个多胺转运系统,便于外源性多胺进入细胞内。这个系统在高速增值的细胞中有非常高的活性,并且是目前正在开发的一些化疗药物的目标。[3]
多胺也是许多离子通道的重要调节剂,包含NMDA受体、AMPA受体。它们阻止内向整流钾离子通道,让通道的电流内向整流,使细胞能量(即穿过细胞膜的K+
离子梯度)守恒。此外多胺也会参与启动大肠杆菌素E7操纵子和SOS反应中下调的蛋白质,这对大肠杆菌素E7的摄取是必须的,并对处于严峻生长条件中的大肠杆菌提供优势。[4]
多胺在植物衰老中参与调节,所以被认为是一种植物激素。[5]另外,它们会直接参与细胞死亡的调节[6],也可以增强血脑屏障的通透性。[7]
螯合剂

多胺是重要的螯合剂。像是四甲基乙二胺(TMED)可以在有机溶剂中溶解金属离子,二乙烯三胺和三乙烯四胺(TETA)和更强大的螯合剂可以分别形成三齿和四齿的复合物,大环多胺可以添加腔选择性的螯合效应,在血红蛋白中的血红素基团是一个大环多胺配体的重要范例。脂肪族线性多胺的芳香族类似物,像是联吡啶、邻二氮菲、三联吡啶也是有用的螯合剂。
质子化的多胺,尤其是大环多胺,可以绑定阴离子。透过改变腔的形状、大小,质子化的多胺可以变为更特殊的阴离子受体。
线性多胺合成
腐胺
腐胺在生物学上可以透过两种不同的途径合成,但起始物都是精氨酸。
尸胺

亚精胺和精胺

多胺类似物
多胺作为在细胞生长中的一个关键角色,导致了一些多胺代谢干扰剂的开发,这些药剂被用于治疗癌症。多胺类似物在细胞内上调p53(肿瘤抑制蛋白)来限制细胞增殖和细胞凋亡。[9]另外它也降低了阳性乳腺癌中的雌激素受体α的表达。[10]
参考资料
- ^ Lawrence, Stephen A. Amines: synthesis, properties and applications. Cambridge University Press. 2004: 64 [2015-01-19]. ISBN 978-0-521-78284-5. (原始内容存档于2016-05-07).
- ^ Rato C, Amirova S.R, Bates D.G, Stansfield I, Wallace H.M. Translational recoding as a feedback controller: systems approaches reveal polyamine-specific effects on the antizyme ribosomal frameshift. Nucleic Acid Res. June 2011, 39 (11): 4587–4597. PMC 3113565
 . PMID 21303766. doi:10.1093/nar/gkq1349.
. PMID 21303766. doi:10.1093/nar/gkq1349.
- ^ Wang C; Delcros JG; Cannon L; et al. Defining the molecular requirements for the selective delivery of polyamine conjugates into cells containing active polyamine transporters. J. Med. Chem. November 2003, 46 (24): 5129–38. PMID 14613316. doi:10.1021/jm030223a.
- ^ Yi-Hsuan Pan, Chen-Chung Liao. The critical roles of polyamines regulating ColE7 production and restricting ColE7 uptake of the colicin-producing Escherichia coli. JBC. May 2006, 281 (19): 13083–13091 [2015-01-19]. PMID 16549429. doi:10.1074/jbc.M511365200. (原始内容存档于2018-11-01).
- ^ Pandey S, Ranade SA, Nagar PK, Kumar N. Role of polyamines and ethylene as modulators of plant senescence. J. Biosci. September 2000, 25 (3): 291–9. PMID 11022232. doi:10.1007/BF02703938.[永久失效链接]
- ^ Moschou, PN; Roubelakis-Angelakis, KA. Polyamines and programmed cell death.. Journal of Experimental Botany. Nov 11, 2013. PMID 24218329. doi:10.1093/jxb/ert373.
- ^ Zhang L, Lee HK, Pruess TH, White HS, Bulaj G. Synthesis and applications of polyamine amino acid residues: improving the bioactivity of an analgesic neuropeptide, neurotensin. J. Med. Chem. March 2009, 52 (6): 1514–7 [2015-01-19]. PMC 2694617
 . PMID 19236044. doi:10.1021/jm801481y. (原始内容存档于2019-11-29).
. PMID 19236044. doi:10.1021/jm801481y. (原始内容存档于2019-11-29).
- ^ Srivenugopal KS, Adiga PR. Enzymic conversion of agmatine to putrescine in Lathyrus sativus seedlings. Purification and properties of a multifunctional enzyme (putrescine synthase). 256 (18): 9532–41. September 1981. PMID 6895223.
- ^ Role of p53/p21(Waf1/Cip1) in the regulation of polyamine analogue-induced growth inhibition and cell death in human breast cancer cells. [21 November 2012]. (原始内容存档于2019-11-29).
- ^ Polyamine analogues down-regulate estrogen receptor alpha expression in human breast cancer cells. [21 November 2012]. (原始内容存档于2019-11-28).
Text is available under the CC BY-SA 4.0 license; additional terms may apply.
Images, videos and audio are available under their respective licenses.
