Oktogén
| Oktogén | |
 | |
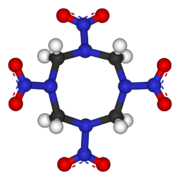 | |
| Všeobecné vlastnosti | |
| Sumárny vzorec | C4H8N8O8 |
| Systematický názov | 1,3,5,7-Tetranitro-1,3,5,7-tetraazacyklooktán |
| Fyzikálne vlastnosti | |
| Molárna hmotnosť | 296,155 g/mol |
| Teplota topenia | 278,5-280 °C |
| Ďalšie informácie | |
| Číslo CAS | 2691-41-0 |
| Pokiaľ je to možné a bežné, používame jednotky sústavy SI. Ak nie je hore uvedené inak, údaje sú za normálnych podmienok. | |
| Výbušné vlastnosti | |
| Detonačná rýchlosť | 7100 ms-1 pri 1,35 gcm-3
9100 ms-1 pri 1,84 gcm-3 |
| Detonačný tlak | ~45 GPa (orientačne) |
| Výbuchová teplota | 4031 °C |
| Výbuchové teplo | 5675 kJkg-1 |
| Objem plynov | 927 dm3kg-1 |
| Pracovná schopnosť v olovenom valci | 450-480 cm3
153 % TNT |
| Pracovná schopnosť v balistickom mažiari |
150 % TNT |
| Brizancia (podľa Kasta) | pri hustote 1,83 g/cm³ — 5,4 mm |
| Citlivosť na náraz (podľa Kasta) | 32 cm, 2 kg |
| Teplota vzbuchu | 335-337 °C (vzbuch do 5 sec) |
Oktogén je veľmi výkonná trhavina, na vojenské a špeciálne použitie.
Vlastnosti
[upraviť | upraviť zdroj]Oktogén v čistej forme je bezfarebná/biela kryštalická látka, ktorá má štyri kryštalické modifikácie - α, β, γ, δ, ale len β modifikácia (ortorombická, podobná kryštálom hexogénu) je stabilná pri normálnej teplote. Je nerozpustný vo vode a málo rozpustný vo väčšine organických rozpúšťadiel (rozpúšťa sa menej než hexogén). Rozpúšťa sa v kyseline dusičnej. Vďaka malej rozpustnosti je málo jedovatý.
Oktogén je chemicky odolný voči kyselinám s nízkou koncentráciou. Alkalické látky spôsobujú rýchlu hydrolýzu oktogénu, už 1% roztok uhličitanu sodného rozkladá oktogén, zvlášť pri teplote varu. Voči hydroxidu sodnému je oktogén odolnejší ako hexogén, čo sa dá využiť pri čistení oktogénu.
Použitie
[upraviť | upraviť zdroj]Oktogén vzniká pri takmer všetkých postupoch výroby hexogénu a naopak. Pri výrobe hexogénu sa nemusí oktogén odstraňovať, pretože má síce o niečo menšiu pracovnú schopnosť, ale vyššiu detonačnú rýchlosť a vyššiu stabilitu.
Čistý oktogén je relatívne veľmi drahý a preto sa oktogén v čistej forme používa vzácne. Oveľa častejšie sa používa zmes hexogénu a oktogénu. Používa sa ako trhavá náplň kumulatívnych striel (obvykle v zmesiach trhavín) a na prípravu špeciálnych, zmesných, a plastických trhavín. Bleskovica plnená oktogénom má detonačnú rýchlosť 6500ms-1 a je plne použiteľná pri teplote až 220°C.
Používa sa aj ako súčasť vysokovýkonných tuhých raketových palív.
Výroba oktogénu
[upraviť | upraviť zdroj]Oktogén sa dá pripraviť z hexamínu a kyseliny dusičnej za prítomnosti acetanhydridu a kyseliny octovej. V prvom kroku vzniká pri teplote 15-30°C látka označovaná ako DPT (dinitropentametyléntetramín) (výťažok 20%). V druhom kroku je DPT podrobená nitrolýze kyselinou dusičnou za prítomnosti dusičnanu amónneho a acetanhydridu pri teplote 60-65°C a vzniká oktogén (výťažok 80%).
Zmes hexogénu a oktogénu, relatívne bohatá na oktogén, sa pripravuje z hexamínu, dusičnanu amónneho a kyseliny dusičnej (v Nemecku zavedený proces KA, vypracovaný v roku 1943 Knöfflerom). Úpravou reakčných podmienok vzniká zmes, ktorá obsahuje až 10% oktogénu.
Podobne pri výrobe hexogénu "procesom E" vzniká zmes, ktorá obsahuje 6% oktogénu.
Čistenie oktogénu od hexogénu je možné niekoľkými spôsobmi. Napríklad je možné využiť vyššiu odolnosť oktogénu voči rozkladu hydroxidom sodným - zmes oktogénu a hexogénu sa zahrieva s hydroxidom sodným za takých podmienok, aby sa hexogén rozložil, ale oktogén nie.
Iný postup delenia využíva rozdielnu rozpustnosť oktogénu a hexogénu v kyseline dusičnej HNO3. Zmes RDX a HMX sa zahrieva v 55% kyseline dusičnej a filtruje. Z filtrátu sa ďalej pomocou 2-nitropropánu extrahuje hexogén, oktogén sa v 2-nitropropáne nerozpúšťa. Oktogén sa nakoniec vyčistí rekryštalizáciou zo 70% HNO3
Je možné aj čistenie rekryštalizácou z cyklopentánu.
Text is available under the CC BY-SA 4.0 license; additional terms may apply.
Images, videos and audio are available under their respective licenses.
