Иодид меди(I)
Материал из Википедии — свободной энциклопедии
| Иодид меди(I) | |
|---|---|
  | |
| Систематическое название | Иодид меди(I) |
| Химическая формула | CuI |
| Внешний вид | белые кристаллы, со временем коричневеют |
| Свойства | |
| Молярная масса | 190,45 г/моль |
| Температура плавления | 605 °C (878,15 К) |
| Температура кипения | 1320 °C (1593,15 К) |
| Плотность | 5,62 г/см³ |
| Показатель преломления | 2,346 |
| Твёрдость по Моосу | 2,5 |
| Растворимость в воде | 2⋅10−5 г/100 мл |
| Произведение растворимости | 1,1⋅10−12 |
| Давление пара | 13 гПа (656 °С) |
| Термодинамические свойства | |
| Стандартная энтальпия образования | −68 кДж/моль |
| Стандартная молярная энтропия | +97 Дж/(моль·К) |
| Стандартная энергия образования Гиббса | −70 кДж/моль |
| Классификация | |
| Регистрационный номер CAS | 7681-65-4 |
| Регистрационный номер EC | 231-674-6 |
| Безопасность | |
| R-фразы | R22; R36/37/38; R50/53 |
| S-фразы | S22; S24/25; S26; S61 |
| H-фразы | H302; H315; H319; H335; H340 |
| P-фразы | P261; P273; P305 + P351 + P338 |
| Пиктограммы опасности |
|
| Пиктограммы опасности СГС |
|
| NFPA 704 | |
| Где это не указано, данные приведены при стандартных условиях (25 °C, 100 кПа). | |

Иоди́д ме́ди(I) — неорганическое вещество с формулой , соединение меди и иода. Относится к классу бинарных соединений, может рассматриваться как соль одновалентной меди и иодоводородной кислоты. В чистом виде — белое кристаллическое вещество, со временем приобретает бурый цвет из-за разложения на медь и иод[1].
Нахождение в природе
[править | править код]Иодид меди(I) встречается в природе в виде минерала маршита. Цвет минерала от белого до темно-коричневого. Твёрдость по шкале Мооса 2,5.[2]
Физические свойства
[править | править код]Иодид меди(I) при нормальных условиях — твёрдое вещество белого цвета, нерастворимое в воде, этаноле, эфире, хорошо растворимое в пиридине (до 1,73 моль/кг). Растворяется в диметилформамиде в присутствии молекулярного иода, причем концентрация иодида меди в растворе прямо зависит от концентрации молекулярного иода. Плавится без разложения при 605 °C. Не образует кристаллогидратов[1][3], но с пиридином образует комплексы состава .
Иодид меди(I), как и большинство бинарных соединений с галогенами, является неорганическим полимером. Иодид меди(I) имеет богатую фазовую диаграмму, а это значит, что он существует в нескольких кристаллических формах. Иодид меди(I) принимает структуру сфалерита ниже 390 °C (γ-CuI), структуру вюрцита между 390 и 440 °C (β-CuI) и структуру галита выше 440 °C (α-CuI). Когда иодид меди(I) принимает структуру сфалерита и вюрцита, ионы располагаются тетраэдрически, на расстоянии 2,338 Å. Бромид меди(I) и хлорид меди(I) аналогично переходят из структуры сфалерита в структуру вюрцита при 405 и 435 °C, соответственно. Межатомные расстояния в бромиде меди(I) и хлориде меди(I) равны 2,173 и 2,051 Å соответственно.[4]
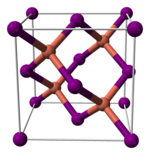 |
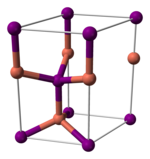 |
 |
Химические свойства
[править | править код]Иодид меди(I) не реагирует с гидратом аммиака; подвергается следующим химическим превращениям[1]:
- Иодид меди медленно окисляется кислородом воздуха до иода, что объясняет его окраску.
- переводится в раствор с помощью реакций ионного обмена с концентрированными растворами иодоводородной кислоты, иодида калия, цианида калия, тиосульфата натрия
- , где
- окисляется до соединений меди(II) и иода концентрированной азотной кислотой, горячей концентрированной серной кислотой
- в горячей концентрированной щёлочи разлагается до оксида меди(I)
- под действием сильных восстановителей (например, алюмогидрид лития) образует гидрид меди(I)
Получение
[править | править код]Иодид меди(I) может быть получен следующими способами:[1]
- взаимодействием оксида меди(I) с разбавленной иодоводородной кислотой
- нагреванием оксида меди(II) с иодидом алюминия
- взаимодействием растворимых солей меди(II) с растворимыми иодидами; образующийся в данной реакции гипотетический иодид меди(II) мгновенно превращается в иодид меди(I)
- взаимодействием металлической меди (например, в виде порошка) с растворами иода в пиридине или диметилформамиде[5]
- В отличие от прочих способов, иодид меди получается в виде раствора в органическом растворителе.
Применение
[править | править код]Индикатор паров ртути.
Токсичность
[править | править код]Вызывает раздражение слизистых оболочек (глаз, органов дыхания). Может вызывать раздражение кожи. При проглатывании вызывает раздражение ЖКТ и общее отравление.
Очень опасно для водных организмов. Может вызывать долговременные негативные изменения в водной среде. LC50 для рыбок Danio rerio составляет 0,4 мг/л в течение 96 ч.
См. также
[править | править код]Примечания
[править | править код]- ↑ 1 2 3 4 Лидин Р. А., Молочко В. А., Андреева Л. Л. Реакции неорганических веществ: справочник / Под ред. Р. А. Лидина. — 2-е изд., перераб. и доп. — М.: Дрофа, 2007. — С. 146—152. — 637 с. — ISBN 978-5-358-01303-2.
- ↑ Маршит на webmineral.com. Дата обращения: 26 июня 2011. Архивировано 7 февраля 2010 года.
- ↑ Лидин Р. А., Андреева Л. Л., Молочко В. А. Константы неорганических веществ: справочник / Под ред. Р. А. Лидина. — 2-е изд., перераб. и доп. — М.: Дрофа, 2006. — С. 103, 604. — 685 с. — ISBN 5-7107-8085-5.
- ↑ Wells, A. F. Structural Inorganic Chemistry Oxford University Press, Oxford, (1984). 5th ed., p. 410 and 444.
- ↑ Калита Д. И. Медь, её сплавы, ртуть и амальгамы в качестве восстановителей в содержащих растворённый иод органических средах: диссертация … кандидата химических наук : 02.00.04.- Курск, 2001.- 169 с.
Text is available under the CC BY-SA 4.0 license; additional terms may apply.
Images, videos and audio are available under their respective licenses.




![{\displaystyle {\mathsf {CuI\ +\ MI\ \longrightarrow \ M[CuI_{2}]))}](https://wikimedia.org/api/rest_v1/media/math/render/svg/7e645a9abb2ac1f59edbd1193181d995fb1a4bfa)

![{\displaystyle {\mathsf {CuI\ +\ 2KCN\ \longrightarrow \ K[Cu(CN)_{2}]\ +\ KI))}](https://wikimedia.org/api/rest_v1/media/math/render/svg/1c5e1113f6eefb18cc1b468e5ee5fb2232653259)
![{\displaystyle {\mathsf {CuI\ +\ 2Na_{2}S_{2}O_{3}\ \longrightarrow \ Na_{3}[Cu(S_{2}O_{3})_{2}]\ +\ NaI))}](https://wikimedia.org/api/rest_v1/media/math/render/svg/c266d3eb786691cbf68fde2ea261e860b0c40ca7)



![{\displaystyle {\mathsf {4CuI\ +\ Li[AlH_{4}]\ \longrightarrow \ LiI\ +\ AlI_{3}\ +\ 4CuH))}](https://wikimedia.org/api/rest_v1/media/math/render/svg/a9bf8ef71d06799045de8936caa5287ad3df419c)


![{\displaystyle {\mathsf {2Cu^{2+}\ +\ 4I^{-}\ \longrightarrow \ 2[CuI_{2}]\ \longrightarrow \ 2CuI\downarrow \ +\ I_{2))))](https://wikimedia.org/api/rest_v1/media/math/render/svg/d598786c93cc37dc4760178b7c3b9d53ae1285e8)

