Сублимация (физика)
Материал из Википедии — свободной энциклопедии


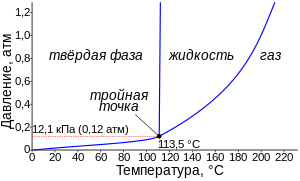
Ниже температуры тройной точки на диаграмме фазового равновесия имеется только линия сублимации. Поэтому при относительно медленном (квазистатическом) нагреве в открытой системе, когда подавляющая часть подводимой от нагревателя энергии расходуется на фазовый переход (возгонку), а не на повышение температуры твёрдой фазы, иод не плавясь возгоняется и превращается сразу в пары. Наоборот, при охлаждении иод десублимируется и образует кристаллы минуя жидкое состояние. Для превращения в жидкость твёрдый иод нагревают в закрытом сосуде. При очень быстром (нестатическом) нагреве иод плавится даже в открытом сосуде.
Сублима́ция (от лат. sublimo «возносить»), возго́нка — переход вещества из твёрдого состояния сразу в парообразное, минуя стадию плавления (перехода в жидкое состояние) и кипения. Поскольку при возгонке изменяется удельный объём вещества и поглощается энергия (теплота сублимации), возгонка является фазовым переходом первого рода[1][2].
Обратным процессом является десублимация — конденсация вещества из парообразного состояния, минуя жидкое, непосредственно в твёрдое состояние[2]. Как и сублимация, десублимация представляет собой фазовый переход первого рода. Десублимация может осуществляться на холодной поверхности или при смешении паров вещества с более холодным газом, при расширении некоторых сжатых газов (образование твёрдого диоксида углерода при работе углекислотных огнетушителей). Примерами десублимации служат такие атмосферные явления, как десублимация атмосферной влаги с образованием инея на поверхности земли и изморози на ветвях деревьев и проводах, морозных узоров на оконных стёклах[1]. Образование и изменение ядер комет также имеет сублимационно-десублимационную природу[2].
Оба процесса — и сублимация, и десублимация — протекают при температуpaх и давлениях ниже тех, что соответствуют тройной точке рассматриваемого вещества[1].
Примеры возгонки
[править | править код]Сублимация иода
[править | править код]Возгонка характерна, например, для элементарного иода I2, который при нормальных условиях не имеет жидкой фазы: чёрные с голубым отливом кристаллы сразу превращаются (сублимируются) в газообразный молекулярный иод (медицинский «иод» представляет собой спиртовой раствор).
Сублимация углекислого газа (сухого льда)
[править | править код]Сухой лёд (твёрдый углекислый газ) является наиболее типичным примером вещества, подвергающегося при нормальном атмосферном давлении возгонке. Температура сублимации углекислого газа составляет 194,65 K (или - 78,5°C), в жидком состоянии диоксид углерода может существовать только при повышенном давлении. Так, при 20°C диоксид углерода переходит в жидкость при давлении более 6 МПа (61.183 кгс/см²).
Сублимация льда
[править | править код]Хорошо поддаётся возгонке лёд, что определило широкое применение данного процесса как одного из способов сушки.
Применение процесса
[править | править код]
1 Вход холодной воды
2 Выход холодной воды
3 Вакуум/газ линия
4 Сублимационная камера
5 Сублимируемый продукт
6 Сырой материал
7 Внешний нагрев
В промышленности сублимацию и десублимацию используют для выделения веществ из газовых потоков (например, фталевого ангидрида, гексафторида урана), очистки веществ, сублимационной сушки (например, пищевых продуктов), тепловой защиты летательных аппаратов при сверхзвуковых скоростях полёта, нанесения защитных и функциональных покрытий при изготовлении приборов и др.[1]
Применение сублимации в лабораторной технике
[править | править код]На эффекте возгонки основан один из способов очистки твёрдых веществ. При определённой температуре одно из веществ в смеси возгоняется с более высокой скоростью, чем другое. Пары очищаемого вещества конденсируют на охлаждаемой поверхности. Прибор, применяемый для этого способа очистки, называется сублиматор.
Сублимационная сушка
[править | править код]Сублимационная сушка (иначе лиофилизация; лиофильная сушка) (англ. freeze drying или lyophilization) — процесс удаления растворителя из замороженных растворов, гелей, суспензий и биологических объектов, основанный на сублимации затвердевшего растворителя (льда) без образования макроколичеств жидкой фазы.
При промышленной возгонке сначала производят заморозку исходного тела, а затем помещают его в вакуумную или заполненную инертными газами камеру. Физически процесс возгонки продолжается до тех пор, пока концентрация водяных паров в камере не достигнет нормального для данной температуры уровня, в связи с чем избыточные водяные пары постоянно откачивают. Возгонка применяется в химической промышленности, в частности, на производствах взрывоопасных или взрывчатых веществ, получаемых осаждением из водных растворов.
Возгонка также используется в пищевой промышленности: так, например, сублимированный кофе получают из замороженного кофейного экстракта через обезвоживание вакуумом. Фрукты после сублимирования весят в несколько раз меньше, а в воде восстанавливаются. Сублимированные продукты значительно превосходят сушёные по пищевой ценности, так как возгонке поддаётся только вода, а при термическом испарении теряются многие полезные вещества.
См. также
[править | править код]- Ассимиляция
- Сублимационный принтер
- Сублимационная печать
Примечания
[править | править код]Литература
[править | править код]- Горелик А. Г. Сублимация // Химическая энциклопедия. — Большая Российская энциклопедия, 1995. — Т. 4. — С. 449—451.
- Раков Э. Г. Сублимация и десублимация // Большая российская энциклопедия. — Большая Российская энциклопедия, 2016. — Т. 31. — С. 361.
Ссылки
[править | править код]Термодинамические состояния вещества | |||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Фазовые состояния |
| ||||||||||||||||
| Фазовые переходы |
| ||||||||||||||||
| Дисперсные системы | |||||||||||||||||
| См. также | |||||||||||||||||
Text is available under the CC BY-SA 4.0 license; additional terms may apply.
Images, videos and audio are available under their respective licenses.
