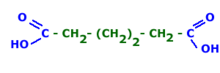Ácido adípico
| Ácido Adípico Alerta sobre risco à saúde | |
|---|---|

| |

| |
| Nome IUPAC | Ácido Hexanodióico |
| Outros nomes | ácido butano - 1,4 - dicarboxílico |
| Identificadores | |
| Número CAS | |
| SMILES |
|
| Propriedades | |
| Fórmula molecular | C6H10O4 |
| Massa molar | 146.14 g/mol |
| Aparência | cristais brancos[1] |
| Densidade | 1.36 g/cm³ |
| Ponto de fusão |
152 °C (425 K) |
| Ponto de ebulição |
337 °C (610 K) |
| Solubilidade em água | pouco solúvel |
| Riscos associados | |
| Principais riscos associados |
Inflamável |
| NFPA 704 | |
| Frases R | R: R36 |
| Ponto de fulgor | 232 °C |
| Compostos relacionados | |
| Outros catiões/cátions | Adipato de sódio Adipato de potássio |
| ácidos dicarboxílicos relacionados | Ácido glutárico (C5) Ácido pimélico (C7) Ácido sacárico (hidroxilas nos carbonos 2,3,4,5) |
| Compostos relacionados | Ácido hexanóico Adipamida (diamida) Cloreto de adipoila Ácido sacárico (ácido (2S,3S,4S,5R)-2,3,4,5-tetraidroxyhexanodioico) |
| Página de dados suplementares | |
| Estrutura e propriedades | n, εr, etc. |
| Dados termodinâmicos | Phase behaviour Solid, liquid, gas |
| Dados espectrais | UV, IV, RMN, EM |
| Exceto onde denotado, os dados referem-se a materiais sob condições normais de temperatura e pressão Referências e avisos gerais sobre esta caixa. Alerta sobre risco à saúde. | |
Ácido adípico é um ácido dicarboxílico de cadeia normal e saturada, que apresenta fórmula estrutural:
- Fórmula molecular: C6H10O4
- Massa Molecular: 146 u
Nomenclatura
[editar | editar código-fonte]- Oficial: Ácido 1,6-hexanodióico
- Usual: Ácido adípico, ácido 1,4-butano-dicarboxílico, ácido haxanodióico
Propriedades
[editar | editar código-fonte]Aparência
Cristais sólidos, branco, sem odor, pouco solúvel e mais denso que a água.
Fórmula molecular
C6H10O4
Físicas
Ponto de Ebulição: 337°C
Ponto de Fusão: 152°C
Índice de Refração: 1.433
Obtenção
[editar | editar código-fonte]É obtido através da oxidação do ciclohexanol ou ciclohexanona com ácido nítrico na presença de catalisadores de cobre e vanádio.
Aplicações e usos
[editar | editar código-fonte]É uma das matérias-primas básicas para as cadeias de produção de poliamidas, poliuretanos base éster, plastificantes e intermediários químicos. Tem aplicações em sistemas de poliuretanos, sínteses orgânicas, polímeros e fibras têxteis de poliamida, lubrificantes, plastificantes, adesivos, tintas e resinas, espumas flexíveis e rígidas, aplicações alimentares e de detergência.
Ácido adípico reage a hexametilenodiamina (HMD) formando o adipato de hexametilenodiamina, também chamado de sal nylon. O sal nylon é o monômero do polímero usalmente conhecido como nylon.
No passado, o acído adípico era materia-prima da hexametilenodiamina, através da sua reação com amônia e ácido fosfórico, formando a chamada adiponitrila (ADN). Esta reação, contudo, caiu em desuso dado o baixo rendimento, desenvolvimento de processos mais econômicos de produção de ADN (via do butadieno e ácido cianídrico) e crescimento do próprio mercado de ácido adípico.
O ácido adípico também é usado como acidulante na indústria de alimentos, porém seu alto custo de produção não o torna competitivo frente ao ácido cítrico.
Subprodutos da produção de ácido adípico são os diácidos menores, o ácido glutárico (COOH - (CH2)3 - COOH) e ácido succínico (COOH - (CH2)2 - COOH), utilizados como desencalantes em curtumes ou na preparação de solventes pesados (ésteres de glutarato e succinato).
A produção de ácido adípico é também uma grande geradora de monóxido de dinitrogênio ou gás nitroso (N2O), gás gerador de efeito estufa, com um potencial equivalente a 310 toneladas de CO2 por tonelada de N2O.
Curiosidades
[editar | editar código-fonte]Referências
- ↑ Mac Gillavry, C. H. (2010). «The crystal structure of adipic acid». Recueil des Travaux Chimiques des Pays-Bas. 60 (8): 605. doi:10.1002/recl.19410600805
Text is available under the CC BY-SA 4.0 license; additional terms may apply.
Images, videos and audio are available under their respective licenses.