Mangaan(II)nitraat
| Mangaan(II)nitraat | ||||||
|---|---|---|---|---|---|---|
| Structuurformule en molecuulmodel | ||||||
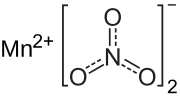
| ||||||
Structuurformule van mangaan(II)nitraat
| ||||||
| Algemeen | ||||||
| Molecuulformule | Mn(NO3)2 | |||||
| IUPAC-naam | mangaan(II)nitraat | |||||
| Molmassa | 178,947849 g/mol | |||||
| SMILES | [N+](=O)([O-])[O-].[N+](=O)([O-])[O-].[Mn+2]
| |||||
| InChI | 1S/Mn.2NO3/c;2*2-1(3)4/q+2;2*-1
| |||||
| CAS-nummer | 10377-66-9 | |||||
| EG-nummer | 233-828-8 | |||||
| PubChem | 61511 | |||||
| Wikidata | Q421490 | |||||
| Waarschuwingen en veiligheidsmaatregelen | ||||||
| ||||||
| H-zinnen | H272 - H302 - H314 - H373 - H412 | |||||
| EUH-zinnen | EUH071 | |||||
| P-zinnen | P220 - P261 - P305+P351+P338 | |||||
| Hygroscopisch? | ja | |||||
| VN-nummer | 2724 | |||||
| Fysische eigenschappen | ||||||
| Aggregatietoestand | vast | |||||
| Kleur | wit | |||||
| Dichtheid | 2,13 g/cm³ | |||||
| Smeltpunt | 37 °C | |||||
| Kookpunt | 129 °C | |||||
| Oplosbaarheid in water | (bij 20°C) 3800 g/L | |||||
| Goed oplosbaar in | water | |||||
| Tenzij anders vermeld zijn standaardomstandigheden gebruikt (298,15 K of 25 °C, 1 bar). | ||||||
| ||||||
Mangaan(II)nitraat is een mangaanzout van salpeterzuur, met als brutoformule Mn(NO3)2. De stof komt voor als een wit kristallijn poeder, dat uiterst goed oplosbaar is in water. Mangaan(II)nitraat is hygroscopisch en vormt bij contact met vocht het donkerroze tetrahydraat. Ook het mono- en het hexahydraat komen voor. Commercieel wordt het zout, dat een zeer laag smeltpunt (37°C) heeft, vaak als oplossing in verdund salpeterzuur verkocht.
Synthese
[bewerken | brontekst bewerken]Mangaan(II)nitraat kan bereid worden door reactie van mangaan(II)carbonaat met salpeterzuur:
Daarnaast kan het ook bereid worden door reactie van mangaan(IV)oxide en stikstofdioxide.
Toepassingen
[bewerken | brontekst bewerken]Mangaan(II)nitraat wordt in laboratoria gebruikt om andere mangaanverbindingen aan te maken, meestal hoogzuivere mangaanoxiden. Daarnaast wordt het ook als kleurstof voor porselein aangewend.
Text is available under the CC BY-SA 4.0 license; additional terms may apply.
Images, videos and audio are available under their respective licenses.






