Asid klorus

| |
| |
| Nama | |
|---|---|
| Nama IUPAC
Chlorous acid
| |
| Nama lain
asid klorik(III)
| |
| Sifat | |
| HClO2 | |
| Jisim molar | 68.46 |
| Keasidan (pKa) | 1.96 |
Kecuali jika dinyatakan sebaliknya, data diberikan untuk bahan-bahan dalam keadaan piawainya (pada 25 °C [77 °F], 100 kPa). | |
| Rujukan kotak info | |
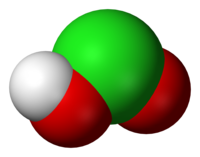
Asid klorus ialah oksoasid klorin(III) yang ada formula kimia HClO2,ialah sejenis asid lemah tetapi ia pengoksidaan kuat dalam asid.Asid klorus adalah sangat tidak stabil dan mudah reput seperti asid hidroklorik,asid klorik dan klorin dioksida.Garam asid klorus ——klorit adalah stabil berbanding dengan asid klorus.Natrium klorit ialah bahan yang untuk menghasilkan klorin dioksida.
HClO2 boleh dihasilkan dengan bertindak balas barium klorit dan asid sulfurik:
- Ba(ClO2)2 + H2SO4 → BaSO4 + 2HClO2
Lihat juga
[sunting | sunting sumber]- klorit—natrium klorit、barium klorit
- asid hipoklorus、asid klorik、asid perklorik
- asid bromus
Rujukan
[sunting | sunting sumber]![]() Kategori berkenaan Asid klorus di Wikimedia Commons
Kategori berkenaan Asid klorus di Wikimedia Commons
- Greenwood, Norman N.; Earnshaw, A. (1997), Chemistry of the Elements (ed. 2nd), Oxford: Butterworth-Heinemann, ISBN 0-7506-3365-4CS1 maint: multiple names: authors list (link)
Sebatian klorin | |
|---|---|
| Asid | |
| Fluorida |
|
| Oksida | |
| Oksifluorida |
|
Lihat juga: Klorida | |
Text is available under the CC BY-SA 4.0 license; additional terms may apply.
Images, videos and audio are available under their respective licenses.
