Diisopropilamina
| Diisopropilamina | ||
|---|---|---|
 | ||
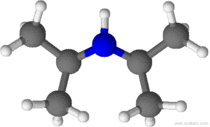 | ||
| Nombre IUPAC | ||
| N-isopropil-2-propanamina | ||
| General | ||
| Otros nombres | N-(1-metiletil)-2-propanamina | |
| Fórmula semidesarrollada | (CH3)2CH-NH-CH(CH3)2 | |
| Fórmula molecular | C6H15N | |
| Identificadores | ||
| Número CAS | 108-18-9[1] | |
| Número RTECS | IM4025000 | |
| ChEMBL | CHEMBL1450356 | |
| ChemSpider | 7624 | |
| PubChem | 7912 | |
| UNII | BR9JLI40NO | |
|
CC(C)NC(C)C
| ||
| Propiedades físicas | ||
| Apariencia | Líquido incoloro. | |
| Olor | Amoníaco o pescado. | |
| Densidad | 718 kg/m³; 0,718 g/cm³ | |
| Masa molar | 10 119 g/mol | |
| Punto de fusión | −61 °C (212 K) | |
| Punto de ebullición | 84 °C (357 K) | |
| Temperatura crítica | 249 °C (522 K) | |
| Presión crítica | 30 atm | |
| Presión de vapor | 79,4 mmHg | |
| Viscosidad | 0,40 cP | |
| Índice de refracción (nD) | 1,392 | |
| Propiedades químicas | ||
| Acidez | 11,07 pKa | |
| Solubilidad en agua | 100 g/L | |
| log P | 1,4 | |
| Familia | Amina | |
| Peligrosidad | ||
| Punto de inflamabilidad | 266,15 K (−7 °C) | |
| Temperatura de autoignición | 589,15 K (316 °C) | |
| Límites de explosividad | 1,1% - 7,1% | |
| Compuestos relacionados | ||
| Aminas |
1-hexanamina Dipropilamina Tripropilamina Dialilamina | |
| Diaminas | 1,6-hexanodiamina | |
| Valores en el SI y en condiciones estándar (25 ℃ y 1 atm), salvo que se indique lo contrario. | ||
La diisopropilamina, también llamada N-(1-metiletil)-2-propanamina, es una amina secundaria de fórmula molecular C6H15N.
Propiedades físicas y químicas
[editar]A temperatura ambiente, la diisopropilamina es un líquido incoloro con olor a amoníaco o pescado. Solidifica a -61 °C y hierve a 84 °C. Posee una densidad de 0,718 g/cm³,[2] inferior a la de otras hexanaminas.
A diferencia de la 1-hexanamina, es un compuesto algo soluble agua, en proporción de 100 g/L. Asimismo, es muy soluble en acetona, benceno, éter y etanol. El valor del logaritmo de su coeficiente de reparto, logP = 1,4, indica que su solubilidad es mayor en disolventes hidrófobos (como el 1-octanol) que en disolventes hidrófilos. Posee una tensión superficial baja —19,6 dina/cm—, comparable a la de alcanos como el hexano y apenas una cuarta parte de la del agua.[3]
La diisopropilamina es una base fuerte (pKa = 11,07), por lo que reacciona violentamente con ácidos fuertes. Asimismo reacciona de forma enérgica con agentes oxidantes, con peligro de fuego o explosión.[4] Puede atacar ciertos tipos de plástico.[3]
Síntesis y usos
[editar]La diisopropilamina puede sintetizarse por la aminación reductora de acetona con amoníaco usando óxido de cobre modificado como catalizador:[5][6]
- NH
3 + 2(CH
3)
2CO + 2H
2 → C
6H
15N + 2H
2O
Por otra parte, la diisopropilamina se usa como precursor de dos herbicidas, dialato y trialato, así como de algunas sulfenamidas utilizadas en la vulcanización del caucho.[7] También se utiliza para fabricar N,N-diisopropiletilamina (Base de Hünig) por alquilación de sulfato de dietilo.[8]
Un haluro de esta amina, el bromuro de diisopropilamonio, es un sólido molecular cuyos cristales son ferroeléctricos a temperatura ambiente.[9] Ello le convierte en una alternativa posiblemente más inerte para el medio ambiente que el titanato de bario, utilizado en condensadores, micrófonos y transductores.
La diisopropilamina es también importante como base conjugada de su derivado de litio, diisopropilamida de litio —también conocido como LDA—, base extremadamente fuerte (pKa = 36) usada en química orgánica para la deprotonación de compuestos débilmente ácidos.
Precauciones
[editar]La diisopropilamina es un material muy inflamable que, al arder, emite gases tóxicos; la mezcla de su vapor con el aire conlleva riesgo de explosión. Tiene su punto de inflamabilidad a -7 °C[2] y alcanza su temperatura de autoignición a 316 °C.[3]
En el organismo humano, la inhalación de vapores de esta amina provoca irritación, a veces con náuseas y vómitos, pudiendo ocasionar quemaduras en las vías respiratorias. Su ingestión también causa irritación en la boca y el estómago. En forma líquida, la diisopropilamina ocasiona quemaduras graves, de tipo cáustico.[3]
Véase también
[editar]Los siguientes compuestos son isómeros de la diisopropilamina:
- 1-hexanamina
- Trietilamina
- Dipropilamina
- 3,3-dimetil-2-butanamina
- 1,3-dimetilbutilamina
- N,N,-dimetilbutilamina
Referencias
[editar]- ↑ Número CAS
- ↑ a b Diisopropylamine (ChemSpider)
- ↑ a b c d Diisopropylamine (PubChem)
- ↑ Diisopropylamine (Chemical Book)
- ↑ Karl Löffler. «Über eine neue Bildungsweise primärer und sekundärer Amine aus Ketonen». Berichte 43 (2): 2031–2035. doi:10.1002/cber.191004302145.
- ↑ One-step process for preparing diisopropylamine Patente US 2686811 A
- ↑ Karsten Eller, Erhard Henkes, Roland Rossbacher, Hartmut Höke "Amines, Aliphatic" Ullmann's Encyclopedia of Industrial Chemistry, 2000, Wiley-VCH, Weinheim. doi 10.1002/14356007.a02_001
- ↑ Hünig, S.; Kiessel, M. (1958). «Spezifische Protonenacceptoren als Hilfsbasen bei Alkylierungs- und Dehydrohalogenierungsreaktionen». Chemische Berichte 91 (2): 380-392. doi:10.1002/cber.19580910223.
- ↑ «An organic alternative to oxides? Organic ferroelectric molecule shows promise for memory chips, sensors». phys.org. 24 de enero de 2013.
Text is available under the CC BY-SA 4.0 license; additional terms may apply.
Images, videos and audio are available under their respective licenses.
