Kalia selenito
| Kalia selenito | ||||
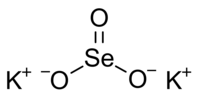 | ||||
| Plata kemia strukturo de la Kalia selenito | ||||
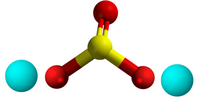 | ||||
| Tridimensia kemia strukturo de la Kalia selenito | ||||
| Alternativa(j) nomo(j) | ||||
| ||||
| Kemia formulo | ||||
| CAS-numero-kodo | 10431-47-7 | |||
| ChemSpider kodo | 132400 | |||
| PubChem-kodo | 150192 | |||
| Fizikaj proprecoj | ||||
| Aspekto | blanka higroskopa pulvoro | |||
| Molmaso | 205.165 g·mol−1 | |||
| Denseco | 2.851g cm−3 | |||
| Fandpunkto | 875 °C | |||
| Mortiga dozo (LD50) | 7 mg/kg (buŝe) | |||
| Sekurecaj Indikoj | ||||
| Riskoj | R23/25 R33 R50/53 | |||
| Sekureco | S28 S36/37 S45 S61 | |||
| Pridanĝeraj indikoj | ||||
| Danĝero
| ||||
| GHS Damaĝo Piktogramo |
| |||
| GHS Signalvorto | Damaĝa substanco | |||
| GHS Deklaroj pri damaĝoj | H301, H331, H373, H400, H410 | |||
| GHS Deklaroj pri antaŭgardoj | P260, P261, P264, P270, P271, P273, P301+310, P304+340, P311, P314, P321, P330, P391, P403+233, P405, P501[1] | |||
(25 °C kaj 100 kPa) | ||||
Kalia selenito aŭ K2SeO3 estas neorganika kombinaĵo de kalio kaj selenita acido, senkolora aŭ blanka solidaĵo kun bazaj proprecoj kaj malforte redukta agado. Ĝi estas solvebla en akvo kaj la rezulta solvaĵo enhavas moderajn koncentriĝojn de hidroksidaj jonoj kaj havas pH-on pli granda ol 7.
Ĝi reakcias kiel bazo por neŭtraligi acidojn. Ĉi-neŭtraligoj generas varmon, sed malpli aŭ ege malpli ol tiu generata per neŭtraligo de bazoj de la Grupo 10[2]. aŭ per neŭtraligo de aminoj. Ĝenerale selenitoj ne agas kiel oksidigaj agentoj aŭ reduktagentoj, sed tiaj kondutoj ne estas neeblaj.
Sintezo 1
[redakti | redakti fonton]- Dissolvado de selena duoksido en diluita solvaĵo de kalia hidroksido
|
|
Sintezo 2
[redakti | redakti fonton]- Interagado de selenita acido kaj koncentrita solvaĵo de kalia hidroksido:
|
|
Sintezo 3
[redakti | redakti fonton]- Malkomponiĝo de kalia selenato:
|
|
Sintezo 4
[redakti | redakti fonton]- Nilson preparis kalian seleniton varmigante egalvalorajn molekulkvantojn de kalia karbonato kaj selena duoksido[3]:
|
|
Reakcioj
[redakti | redakti fonton]Reakcio 1
[redakti | redakti fonton]- Ĝi malkomponiĝas kiam hejtata:
|
|
Reakcio 2
[redakti | redakti fonton]- La kristala anhidra salo prepariĝas per vakua elsekigo:
|
|
Reakcio 3
[redakti | redakti fonton]- Kiam hejtataj, ĝiaj koncentritaj solvaĵoj estigas kalia piro-seleniton kaj kalian hidroksidon:
|
|
Reakcio 4
[redakti | redakti fonton]- Ĝi estas forta oksidigagento:
|
|
Reakcio 5
[redakti | redakti fonton]- Kun hidrogena peroksido ĝi oksidiĝas al kalia selenato:
|
|
Reakcio 6
[redakti | redakti fonton]- Ĝi estas oksidigata de la atmosfera oksigeno:
|
|
Reakcio 7
[redakti | redakti fonton]- Ĝi estas reduktata de la hidrogeno:
|
|
Reakcio 8
[redakti | redakti fonton]- Ĝi partoprenas en reakcio de duobla interŝanĝo kun arĝenta nitrato:
|
|
Reakcio 9
[redakti | redakti fonton]- Alternative, oni povas oksidigi kalian seleniton al kalia selenato en ĉeesto de bromo.[4]
|
|
Literaturo
[redakti | redakti fonton]- Alfa Aesar
- Chemical Book
- Selenium: Geobotany, Biochemistry, Toxicity, and Nutrition
- Toxicological Profile for Selenium
- The Quarterly Journal of the Chemical Society of London
Referencoj
[redakti | redakti fonton]- ↑ Pubchem
- ↑ En la perioda tabelo, la grupo 10 prezentas la jenajn elementojn: nikelo, paladio kaj plateno.
- ↑ The Air Oxidation of Selenium and the Selenites
- ↑ https://books.google.de/books?id=dLLfBAAAQBAJ&pg=PA305#v=onepage&q&f=false
| ||||||
Text is available under the CC BY-SA 4.0 license; additional terms may apply.
Images, videos and audio are available under their respective licenses.



















