Carbidopa
aus Wikipedia, der freien Enzyklopädie
| Strukturformel | ||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
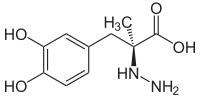
| ||||||||||||||||||||||
| Allgemeines | ||||||||||||||||||||||
| Freiname | Carbidopa | |||||||||||||||||||||
| Andere Namen | ||||||||||||||||||||||
| Summenformel |
| |||||||||||||||||||||
| Kurzbeschreibung |
weißes bis gelblich weißes Pulver (Carbidopa·Monohydrat)[1] | |||||||||||||||||||||
| Externe Identifikatoren/Datenbanken | ||||||||||||||||||||||
| ||||||||||||||||||||||
| Arzneistoffangaben | ||||||||||||||||||||||
| ATC-Code | ||||||||||||||||||||||
| Wirkstoffklasse |
L-DOPA-Decarboxylasehemmer | |||||||||||||||||||||
| Eigenschaften | ||||||||||||||||||||||
| Molare Masse | ||||||||||||||||||||||
| Aggregatzustand |
fest | |||||||||||||||||||||
| Schmelzpunkt | ||||||||||||||||||||||
| Löslichkeit |
schwer löslich in Wasser, sehr schwer löslich in Ethanol, praktisch unlöslich in Dichlormethan, löslich in verdünnten Mineralsäuren (Carbidopa·Monohydrat) [1] | |||||||||||||||||||||
| Sicherheitshinweise | ||||||||||||||||||||||
| ||||||||||||||||||||||
| Toxikologische Daten | ||||||||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen (0 °C, 1000 hPa). | ||||||||||||||||||||||
Carbidopa ist wie Benserazid ein L-DOPA-Decarboxylasehemmer. Es inhibiert die Metabolisierung von L-DOPA (Levodopa) und wird daher als chiraler enantiomerenreiner Arzneistoff in Kombination mit Levodopa zur Therapie der Parkinson-Krankheit eingesetzt. Carbidopa wurde als Decarboxylase-Inhibitor 1961, 1963, 1969 und 1971 von MSD patentiert und ist in Kombination mit Levodopa als Generikum im Handel.[2] Die Kombination Levodopa + Carbidopa wurde 1977 von der Weltgesundheitsorganisation (WHO) in die Liste der unentbehrlichen Arzneimittel der Weltgesundheitsorganisation aufgenommen.[4]
Pharmakologie
[Bearbeiten | Quelltext bearbeiten]Carbidopa verhindert selektiv die Umwandlung von L-DOPA zu Dopamin in der Peripherie, da es die Blut-Hirn-Schranke nicht durchdringen kann.[5] Damit gibt es u. a. weniger Neigung zu Tachykardie, Nykturie, orthostatische Dysregulation. Mit der Zugabe von Carbidopa muss weniger Levodopa verabreicht werden, da ohne periphere Decarboxylierungshemmung 95 % des verabreichten Levodopas außerhalb des Gehirns decarboxyliert werden würde.
Handelsnamen
[Bearbeiten | Quelltext bearbeiten]- Duodopa (D, A, CH), Isicom (D), Levobeta (D), Levo-C (D), LevoCar (A), LevoCarb (D), Levocomp (D), Levodopa (D), Sinemet (A, CH), Striaton (D) sowie ein Generikum (CH)
(Carbidopa in Kombination mit Levodopa.) - Stalevo (D, A, CH)
(Carbidopa in Kombination mit Levodopa und Entacapon)
Einzelnachweise
[Bearbeiten | Quelltext bearbeiten]- ↑ a b Eintrag Carbidopa-Monohydrat CRS beim Europäisches Direktorat für die Qualität von Arzneimitteln (EDQM), abgerufen am 30. Juli 2010.
- ↑ a b c d Eintrag zu Carbidopa. In: Römpp Online. Georg Thieme Verlag, abgerufen am 10. November 2014.
- ↑ a b Datenblatt Carbidopa, European Pharmacopoeia (EP) Reference Standard bei Sigma-Aldrich, abgerufen am 21. Dezember 2019 (PDF).
- ↑ WHO Model List of Essential Medicines. (PDF; 442 kB) abgerufen am 20. September 2012.
- ↑ Mutschler, Arzneimittelwirkungen, 9. Auflage, Wissenschaftliche Verlagsgesellschaft Stuttgart, 2008, ISBN 978-3-8047-1952-1.
Text is available under the CC BY-SA 4.0 license; additional terms may apply.
Images, videos and audio are available under their respective licenses.
